Dr Martin Juneau, M.D., FRCP
Cardiologue, directeur de l'Observatoire de la prévention de l'Institut de Cardiologie de Montréal. Professeur titulaire de clinique, Faculté de médecine de l'Université de Montréal. / Cardiologist and Director of Prevention Watch, Montreal Heart Institute. Clinical Professor, Faculty of Medicine, University of Montreal.
Voir tous les articles/
En bref
- Bien qu’on recommande un apport nutritionnel en protéines de l’ordre de 0,8-1,0 g par kg par jour, ce qui correspond à environ 10-15% des calories totales, l’apport en protéines est beaucoup plus élevé chez certaines personnes et peut même excéder 20 % des calories.
- L’impact de cet apport élevé en protéines a été examiné en comparant l’effet d’un repas contenant des quantités normales (15 % des calories totales) ou élevées de protéines (22 % des calories) sur la fonction des macrophages, une classe de cellules immunitaires impliquées dans le développement de l’athérosclérose.
- Les résultats indiquent que le repas riche en protéines provoque une suractivation du complexe mTOR des macrophages, qui est corrélée avec une accélération de la formation de plaques d’athérosclérose.
- L’acide aminé leucine, présent préférentiellement dans les protéines de source animale, est capable de reproduire à lui seul cet effet athérogénique de fortes quantités de protéines.
- Un apport très élevé en protéines animales, correspondant environ au double de l’apport recommandé, pourrait donc favoriser le développement de l’athérosclérose et augmenter le risque de maladies cardiovasculaires.
Les protéines sont l’une des composantes les plus importantes de notre alimentation parce qu’elles contiennent des acides aminés essentiels que nous sommes incapables de fabriquer par nous-mêmes et qui doivent absolument être apportés par ce que nous mangeons. Ces acides aminés sont utilisés par notre métabolisme pour fabriquer les dizaines de milliers de protéines différentes qui contribuent toutes à leur façon au fonctionnement optimal de l’être humain, que ce soit comme enzymes, hormones, neurotransmetteurs, protéines structurales, récepteurs ou détecteurs d’agents pathogènes (entre autres). En conséquence, si on a assisté à l’émergence au fil des années de régimes qui réduisent drastiquement l’apport en glucides (le régime cétogène, par exemple) ou en lipides (les régimes véganes faibles en gras), il n’y a pas (et il n’y aura jamais) de régime basé sur une réduction de la quantité de protéines ingérées en deçà des minimums recommandés. Bien au contraire, on assiste plutôt au phénomène inverse, c’est-à-dire que les études observent que la plupart des gens perçoivent les aliments riches en protéines ou ceux auxquels des protéines sont ajoutées comme des « aliments santé » et essaient de « manger plus de protéines ».
Apport nutritionnel recommandé
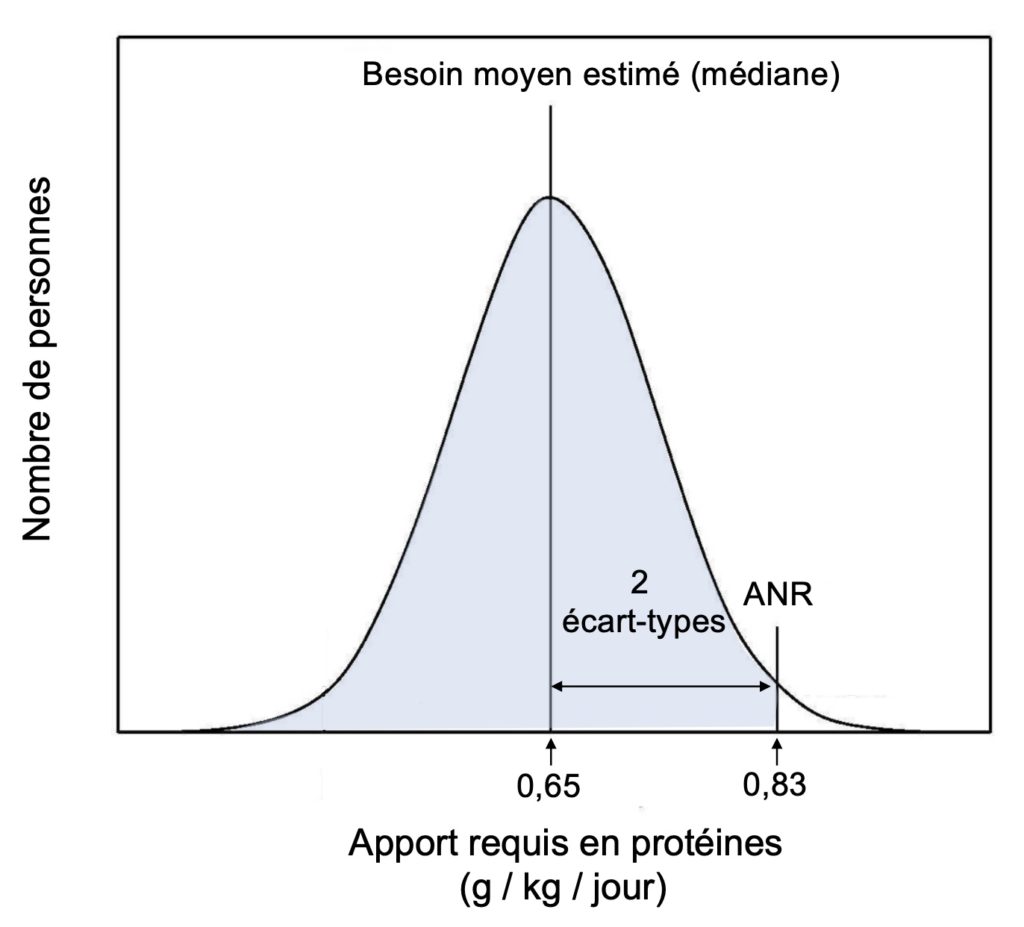
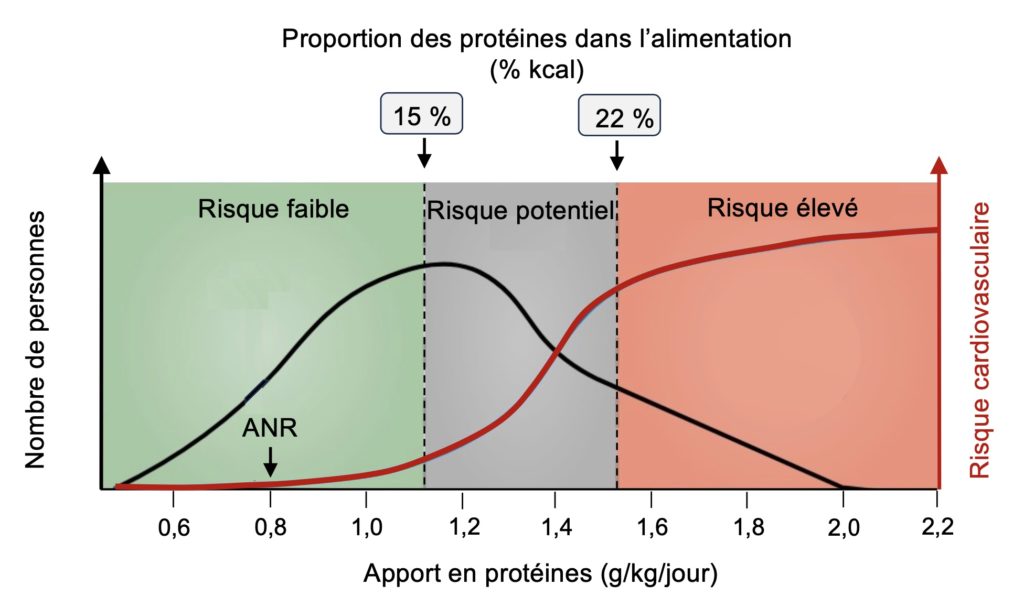
Les quantités requises pour subvenir aux besoins du corps humain en protéines ne sont vraiment pas très difficiles à obtenir. Les études qui se sont penchées sur cette question montrent que l’apport minimal en protéines nécessaire pour contrebalancer les pertes associées au métabolisme normal varie selon les individus, mais qu’une quantité de 0,65 g par kg par jour suffit pour combler les besoins de la moitié (la médiane) de la population. Pour une personne moyenne de 70 kg, cela correspond à seulement 45 g de protéines, soit l’équivalent d’une portion de yogourt pour déjeuner et d’un sandwich au thon au diner. Par contre, puisque la moitié de la population requiert un apport plus élevé en raison de divers facteurs (masse musculaire, niveau d’activité physique, âge), on recommande une quantité de protéines qui correspond à 2 écarts-types de la médiane de façon à couvrir les besoins de 97,5 % des gens (Figure 1). Cet apport nutritionnel recommandé en protéines (0,8 g par kg par jour, soit environ 50 g de protéines pour une personne de 70 kg) représente donc déjà une quantité supérieure aux besoins de base d’une grande partie de la population. Dans les sociétés riches comme la nôtre, les probabilités de présenter une carence en protéines sont donc très faibles.
Beaucoup de protéines
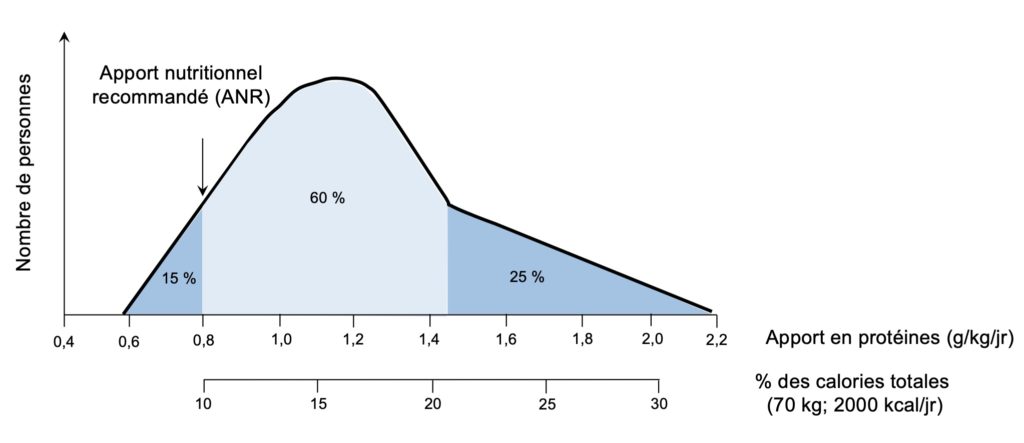
Ceci est particulièrement vrai lorsqu’on examine la distribution de l’apport quotidien en protéines typique de la population nord-américaine (Figure 2). À peine 15 % des individus consomment une quantité de protéines inférieure à l’ANR (mais tout de même supérieure au besoin moyen estimé), tandis que la grande majorité des gens (85%) dépasse ce seuil, avec presque le quart de la population qui consomme même deux fois plus de protéines que les quantités recommandées.
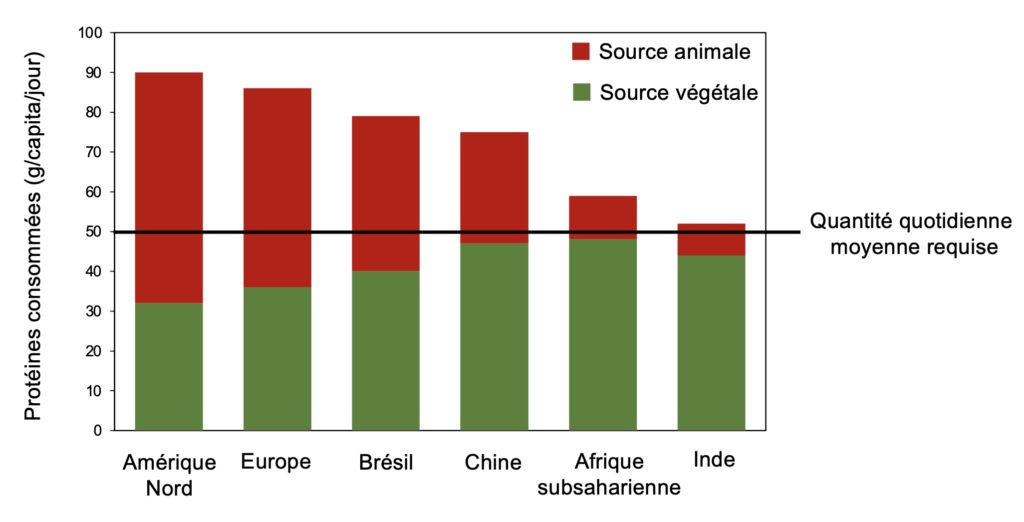
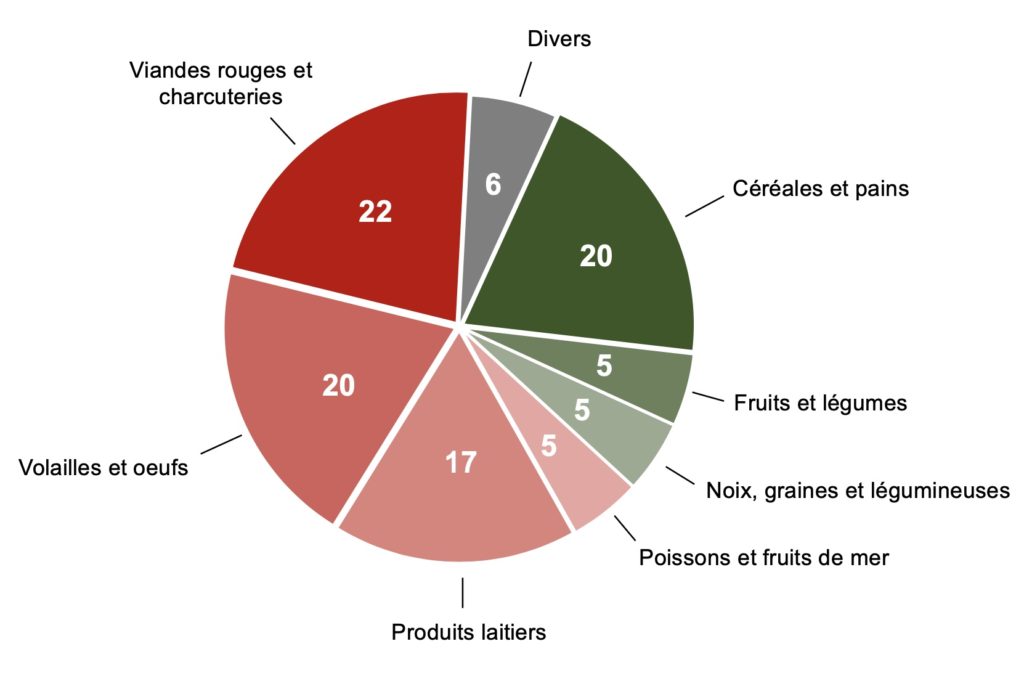
Cette consommation élevée de protéines par les Nord-Américains est bien mise en évidence lorsqu’on la compare avec celle des habitants d’autres régions du globe (Figure 3). En moyenne, l’apport quotidien en protéines est d’environ 90 g par personne, les deux tiers de ces protéines provenant d’aliments de source animale. Au Canada, plus spécifiquement, une étude a établi que la quantité moyenne de protéines consommées est légèrement inférieure à la moyenne nord-américaine (80 vs 90 g par personne), mais que la proportion de protéines d’origine animale est la même, c’est-à-dire que les deux tiers des protéines proviennent des viandes rouges et charcuteries (22%), de la volaille et des œufs (20 %), des produits laitiers (17%) et des poissons et fruits de mer (5%), contre seulement 30 % d’origine végétale (principalement des céréales) (Figure 4).
Globalement, on peut donc voir que nous sommes les plus grands consommateurs de protéines de la planète, en particulier en ce qui concerne les protéines d’origine animale. Il y a plusieurs problèmes associés à l’alimentation occidentale moderne (trop d’aliments ultratransformés, de viandes rouges et pas assez de végétaux et de fibres, par exemple), mais une insuffisance en protéines n’est certainement pas l’un d’eux.
Protéines et masse musculaire
Plusieurs experts estiment qu’une quantité de protéines plus élevée que l’apport recommandé n’est pas dommageable pour les personnes en bonne santé et serait même nécessaire pour les personnes physiquement très actives (1,2 -2 g de protéines par kg recommandé) ou les personnes âgées (>1,2 g par kg par jour).
C’est le maintien ou l’augmentation de la masse musculaire qui représente la principale raison invoquée pour justifier l’importance d’un apport en protéines alimentaires supérieur au seuil recommandé. Notre métabolisme peut stocker l’excédent de sucre (sous forme de glycogène) ou de gras (dans le tissu adipeux), mais ne peut pas faire de réserve de protéines. En cas d’apport insuffisant en protéines, les acides aminés manquants proviennent principalement des muscles, qui contiennent environ 60 % de l’ensemble des protéines présentes dans le corps humain. Ceci est particulièrement problématique pour les personnes âgées qui sont déjà à risque d’être affectées par une diminution de leur masse musculaire (dès l’âge de 50 ans, une perte de la masse musculaire de l’ordre de 0,5 % à 1 % par année est observée) et c’est pour cette raison qu’on préconise un apport plus élevé en protéines chez cette population.
L’incitatif à consommer plus de protéines est particulièrement prononcé chez les personnes qui s’entrainent et doivent récupérer la masse musculaire perdue pendant l’effort ou qui cherchent à augmenter leur musculature et/ou leur puissance musculaire. L’ingestion de protéines stimule effectivement la synthèse de protéines musculaires, mais ce processus atteint rapidement un maximum à 0,25 g/kg chez les 18-37 ans et 0,40 g/kg chez les ≥55 ans. Concrètement, cela signifie qu’il y a une synthèse de nouvelles protéines musculaires jusqu’à des quantités de 18 g par repas pour les jeunes adultes et de 28 g par repas pour les plus âgés, ce qui correspond en gros à l’apport nutritionnel recommandé pour ces deux populations. Au-delà de ces quantités, par contre, les acides aminés (des protéines) en excès sont oxydés, sans possibilité de participer à la synthèse de protéines musculaires. L’ajout de collations protéinées entre les repas n’est pas non plus véritablement une solution, car la synthèse de protéines musculaires demeure réfractaire à la présence de taux sanguins élevés d’acides aminés plusieurs heures après les repas. Autrement dit, même en augmentant la quantité et la fréquence de l’apport en protéines, on se bute rapidement à une saturation du système impliqué dans la synthèse des protéines musculaires et il est donc difficile d’augmenter la masse musculaire simplement en consommant un surplus de protéines. D’ailleurs, un grand nombre d’études ont rapporté qu’un apport en protéines supérieur à l’ANR n’a pas de bénéfice mesurable sur la force musculaire ou la forme physique dans son ensemble.
Trop de protéines ?
Si des quantités de protéines supérieures aux seuils recommandés ne semblent donc pas procurer d’avantages majeurs pour la santé, pourraient-elles au contraire avoir des effets négatifs ? Pour certaines pathologies comme les maladies rénales, la réponse est clairement oui : puisque les reins filtrent et éliminent les déchets du métabolisme des protéines, une diminution de la fonction rénale peut entrainer des lésions et une accumulation de substances toxiques. Chez les personnes en bonne santé, par contre, la tendance actuelle est de considérer que des quantités élevées de protéines n’ont pas d’impacts majeurs sur la santé. Par exemple, l’Institut de médecine (IOM), un organisme indépendant affilié à l’Académie des Sciences américaine, suggère un apport en protéines pouvant varier entre 10-35 % de l’énergie totale, en dépit du fait que des apports ≥15% excèdent de beaucoup l’apport nutritionnel recommandé (pour une personne de 70 kg, l’ANR de 50 g de protéines correspond à 200 calories, soit environ 10 % des calories totales consommées quotidiennement en moyenne).
Cette approche permissive face aux quantités élevées de protéines est un peu étonnante, dans la mesure où plusieurs études réalisées au cours des dernières années ont rapporté qu’un apport excessif de protéines pouvait effectivement avoir des répercussions négatives sur la santé. Par exemple, un grand nombre d’études réalisées sur des modèles animaux(lapin, rongeurs et grands singes, entre autres) ont clairement établi un lien entre un apport élevé en protéines et une accélération de la formation de plaques d’athérosclérose. Un phénomène similaire est possiblement à l’œuvre chez les humains, car une étude suédoise, réalisée auprès de 43396 femmes suivies pendant une quinzaine d’années, a montré qu’un apport protéique élevé était associé à un risque plus élevé de maladies cardiovasculaires.
De plus, au moins huit études populationnelles d’envergure (voir ici et ici, pour des études représentatives) ont rapporté que les grands consommateurs de protéines avaient un risque accru de développer un diabète de type 2 comparativement à ceux qui en mangeaient moins. Cet effet négatif est biologiquement plausible, car il est bien établi que les protéines stimulent la sécrétion d’insuline, tout en interférant avec son signal au niveau des muscles. Sur de longues périodes, cette situation peut produire une résistance à l’insuline et mener avec le temps à un dysfonctionnement du pancréas et à l’apparition d’un diabète de type 2.
Il est important de noter que les hausses du risque de maladies cardiovasculaires et de diabète associées à un apport protéique élevé sont observées pour les protéines animales, mais non pour celles d’origine végétale. C’est donc essentiellement la prédominance des protéines animales (deux tiers des protéines dans les pays occidentaux) qui est responsable de l’effet négatif d’une alimentation riche en protéines sur le risque de développer ces pathologies.
mTOR, le chef d’orchestre de la réponse métabolique aux protéines
Une caractéristique inhérente à une alimentation surchargée en protéines animales est qu’elle apporte des quantités élevées d’acides aminés à chaine latérale ramifiée (leucine, isoleucine et valine) qui sont reconnus comme de puissants activateurs du complexe mTOR (mTORC1). Lorsque ces acides aminés sont présents en quantités élevées, comme lorsque l’apport protéique est supérieur aux seuils recommandés, mTOR est activé et augmente la synthèse des protéines, lipides et nucléotides nécessaires à la croissance. Cette activité est cruciale pour fabriquer les protéines nécessaires au maintien de la masse musculaire, mais une suractivation par mTOR peut néanmoins avoir des répercussions négatives dans d’autres organes du corps et causer des perturbations métaboliques pouvant mener, par exemple, à une résistance à l’insuline (voir notre article à ce sujet).
En parallèle, l’activation de mTOR mène à un blocage de l’autophagie, le processus par lequel la cellule utilise ses propres constituants comme source d’énergie (ce qui permet d’éviter un cycle futile où les nouvelles composantes cellulaires fabriquées en réponse à l’activation de mTOR soient immédiatement dégradées). Cependant, l’autophagie est essentielle pour éliminer les éléments dysfonctionnels qui s’accumulent avec le temps dans les cellules, autant du point de vue des protéines que de constituants plus volumineux, comme les mitochondries (on parle alors de mitophagie). L’inhibition de l’autophagie par un excès de protéines peut donc provoquer une accumulation de structures défectueuses qui interfèrent avec le fonctionnement de la cellule et peuvent éventuellement causer sa mort.
Il est donc possible qu’un apport excessif en protéines d’origine animale, qui dépasse largement les seuils recommandés, puisse exercer des effets négatifs sur certains processus physiologiques (les maladies cardiovasculaires par exemple) en raison de cette suractivation de mTOR.
Protéines et athérosclérose : les macrophages comme intermédiaires
Cette possibilité est appuyée par les résultats d’une étude récente qui montre que des quantités élevées de protéines stimulent le complexe mTOR présent dans une classe de cellules immunitaires, les macrophages, et que ce phénomème est corrélé avec une accélération du développement de l’athérosclérose.
Cette contribution du système immunitaire au processus d’athérosclérose peut sembler à première vue surprenante, étant donné que c’est l’accumulation progressive de dépôts de graisses, notamment le cholestérol transporté par les lipoprotéines de faible densité (LDL), qui est la grande responsable de la formation de ces plaques. D’ailleurs, la réduction des taux sanguins de cholestérol-LDL, soit par des modifications au mode de vie (alimentation, exercice) ou encore par des médicaments (statines), représente encore aujourd’hui l’une des principales interventions utilisées pour freiner le développement de l’athérosclérose et ainsi réduire le risque de ses complications, en particulier l’infarctus du myocarde et l’AVC.
En réalité, cependant, l’athérosclérose est une pathologie beaucoup plus complexe qui ne dépend pas exclusivement des taux sanguins de cholestérol-LDL. En clinique, par exemple, il est bien établi que même en réduisant ces taux de LDL à des niveaux très bas avec des statines, il reste toujours un pourcentage important de patients (presque le quart dans certaines études) qui demeurent à très haut risque de rechutes dans les années suivant le début du traitement. On sait maintenant que ce risque résiduel, indépendant du cholestérol-LDL, est en majeure partie lié à l’inflammation chronique, causée notamment par l’infiltration des macrophages dans la paroi artérielle (Figure 5).

A. L’agression de la couche de cellules endothéliales qui tapissent la paroi interne du vaisseau permet l’entrée et l’oxydation de particules LDL riches en cholestérol à l’intérieur de la paroi. L’effet pro-inflammatoire de cet afflux de lipides oxydés attire les monocytes de la circulation grâce à l’expression de certains récepteurs de surface (VCAM/ICAM-1) qui leur permettent de s’infiltrer à l’intérieur de la paroi. Les monocytes se transforment alors en macrophages et ingèrent par phagocytose les particules LDL oxydées présentes à proximité. Lorsque les quantités de LDL captées par les macrophages sont grandes, ils deviennent surchargés de lipides et se transforment en cellules spumeuses. Cette surcharge est toxique pour les cellules et entrainent leur mort et la relâche des lipides qu’elles contiennent. Ce phénomène entraîne une réaction inflammatoire chronique locale qui stimule la croissance des cellules musculaires présentes dans la paroi du vaisseau, et qui mène à la formation d’une chape fibreuse qui isole les macrophages morts ou en voie de l’être et la matière graisseuse de la circulation sanguine. Ces plaques précoces ne présentent aucun danger immédiat, car la chape fibreuse est très stable et parvient à sceller hermétiquement les dépôts graisseux présents dans la paroi de l’artère.
B. L’agression continue des cellules endothéliales, que ce soit en raison d’une exposition chronique à des quantités élevées de particules LDL ou encore à certains facteurs du mode de vie qui favorise l’inflammation (obésité, sédentarité, tabac), mène avec le temps à une accumulation de cellules spumeuses et à la progression de l’athérosclérose. On observe typiquement un noyau lipidique constitué de cellules mortes et de lipides, incluant des cristaux de cholestérol. Le climat fortement pro-inflammatoire engendré au sein de ce noyau lipidique peut alors déstabiliser la couche fibreuse, provoquant l’apparition de zones très minces et fragiles à la surface de la plaque. La rupture de ces plaques expose alors leur contenu au système de coagulation qui, croyant qu’il s’agit d’une blessure à réparer, forme immédiatement un thrombus (caillot) qui obstrue complètement le vaisseau et mène à un infarctus (blocage des coronaires) ou un AVC (blocage des carotides). Adapté de Chen et coll. (2022).
Tout débute lorsque les cellules endothéliales qui tapissent la paroi des artères sont confrontées à un déséquilibre qui affecte leur fonction (on parle alors de dysfonction endothéliale), qu’il s’agisse d’un excès de particules LDL ou encore de différents stimuli inflammatoires (fumée de cigarette, microorganismes, conditions inflammatoires chroniques liées au mode de vie comme le surpoids et la sédentarité). Il y a alors une perte d’étanchéité de cette couche protectrice qui va faciliter l’entrée des particules LDL et leur oxydation subséquente par les radicaux libres produits par les cellules endothéliales dysfonctionnelles. En parallèle, l’expression de récepteurs à la surface de l’endothélium va permettre à une classe de cellules immunitaires, les monocytes, de se faufiler à l’intérieur de la paroi du vaisseau où elles se transforment en macrophages. Ces macrophages jouent un rôle primordial dans la progression de l’athérosclérose en captant par phagocytose de grandes quantités de LDL oxydées, ce qui les transforme en cellules spumeuses (foam cells) dans lesquelles il est possible d’observer des dépôts de cholestérol (le terme « spumeuse », du latin « spuma » qui signifie « écume », provient de la grande quantité de lipides qu’elles contiennent et qui apparaît comme des « bulles » lors de l’examen des cellules par microscopie).
L’exposition chronique de la paroi des vaisseaux à des conditions qui favorisent l’invasion de la paroi artérielle par les macrophages (mode de vie, certaines prédispositions génétiques) crée avec le temps une accumulation de ces cellules spumeuses et la formation d’un noyau lipidique au centre de la plaque, formé de cholestérol et de débris cellulaires. Le climat très inflammatoire qui règne au sein de cette zone nécrotique peut graduellement déstabiliser la chape fibreuse et la rendre plus fragile et à risque de se fissurer. Lorsque cette rupture se produit, la fuite du contenu de la plaque est perçue par le système de coagulation comme une blessure à colmater, menant alors à l’agrégation des plaquettes, la formation d’un réseau de fibrine et à l’apparition d’un caillot qui va obstruer le passage du sang dans l’artère.
En somme, on peut voir que la progression de l’athérosclérose n’est pas strictement une conséquence de taux élevés de cholestérol : l’inflammation chronique causée par l’accumulation de macrophages saturés de lipides joue elle aussi un rôle primordial dans ce processus. L’activation de ces macrophages pourrait donc représenter un mécanisme biologiquement plausible pour expliquer la hausse du risque de maladies cardiovasculaires associé à un apport élevé en protéines.
Protéines activatrices
Pour déterminer la quantité de protéines alimentaires associée à une activation des macrophages, les chercheurs ont administré à des volontaires deux repas différents, contenant soit 15 % ou 22 % des calories totales sous forme de protéines. Ces quantités ont été choisies parce que l’une d’entre elles (15 %) correspond à l’apport protéique de la majorité des gens, légèrement supérieur aux minimums recommandés, tandis que l’autre (22 %) correspond au double de l’apport recommandé et est représentative de la consommation élevée de protéines par une proportion non négligeable de la population (voir la Figure 2).
L’activité du complexe mTOR dans les monocytes isolés du sang des participants a été par la suite évaluée en mesurant deux réactions qui sont la signature d’un complexe mTOR activé, soit le transfert d’un groupement phosphate sur une enzyme impliquée dans la synthèse de nouvelles protéines et la croissance cellulaire (protéine S6), ainsi que sur une enzyme qui bloque le processus d’autophagie (ULK1) (Figure 6). Les résultats montrent clairement qu’un apport élevé en protéines, largement supérieur à celui qui est recommandé, influence plus fortement l’activité de mTOR, autant en augmentant son effet activateur sur la croissance (phosphorylation de S6) qu’en réduisant le processus d’autophagie des cellules.
Curieusement, même si plusieurs acides aminés sont capables d’activer mTOR, les chercheurs ont observé que la leucine était capable à elle seule de reproduire l’effet des protéines sur l’activation des voies de croissance cellulaire et l’inhibition de l’autophagie (Figure 6C).
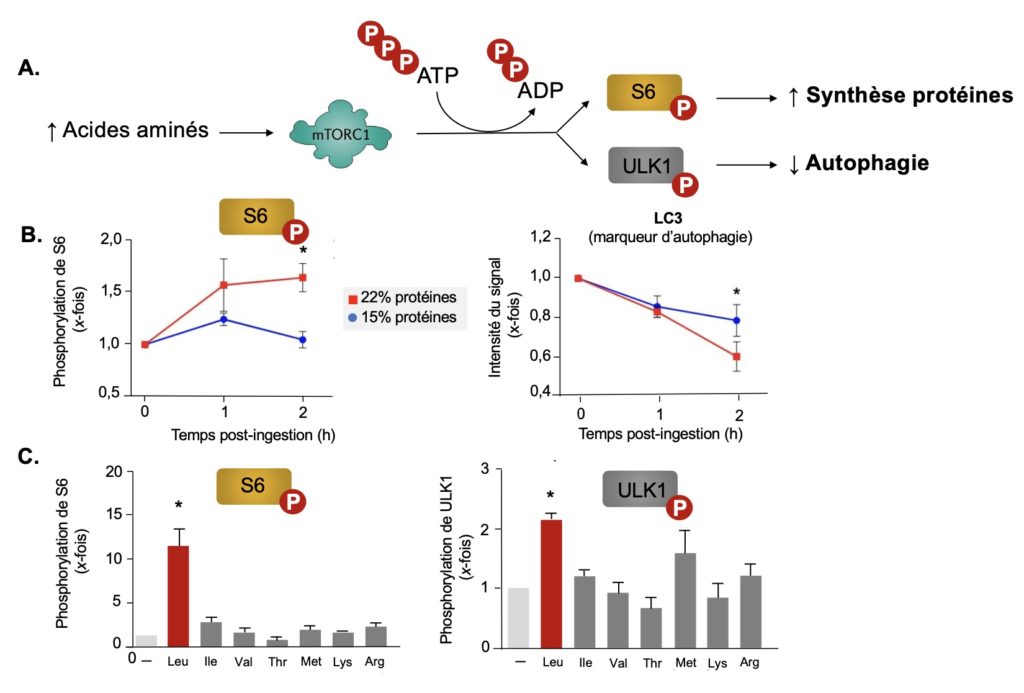
A. Représentation schématique de méthodes servant à mesurer de l’activité de mTORC1 dans les cellules. En réponse à la présence de quantités importantes d’acides aminés provenant de la digestion des protéines, mTOR est activé et transfère un groupement phosphate de l’ATP à certaines protéines de la cellule. La phosphorylation de la protéine S6 participe à la cascade menant à la production de nouvelles protéines et à la croissance, tandis que la phosphorylation de la protéine ULK1 contribue au blocage du processus d’autophagie.
B. Un apport alimentaire élevé en protéines active le complexe mTOR et inhibe l’autophagie dans les monocytes humains. 9 volontaires à jeun ont consommé des repas contenant 15 % ou 22 % des calories totales sous forme de protéines. Les protéines supplémentaires provenaient d’un mélange d’œufs, de poulet, de bœuf et de lactosérum (petit lait). Les monocytes du sang des volontaires ont été isolés juste avant l’intervention ou 1 et 2 heures après l’ingestion des repas et l’activité de mTOR des cellules mesurée par la hausse de phosphorylation de la protéine S6 (graphique de gauche) ou par l’analyse de la répartition à l’intérieur des cellules de la protéine LC3, un marqueur du processus autophagique (graphique de droite).
C. La leucine est le principal acide aminé responsable de l’activation de mTOR induite par un apport élevé en protéines.Des monocytes humains en culture ont été mis en présence de 7 acides aminés dont les concentrations sanguines sont le plus fortement augmentées après l’ingestion d’un repas riche en protéines. L’activité de mTOR a été évaluée par la mesure de la phosphorylation de la protéine S6 (graphique de gauche) ou de la protéine ULK1 (graphique de droite). Les astérisques indiquent une différence statistiquement significative. Tiré de Zhang et coll. (2024).
L’athérosclérose est un processus graduel, dont le développement peut s’échelonner sur plusieurs décennies, et il est donc impossible de quantifier dans une étude de courte durée l’impact d’une alimentation riche en protéines sur l’évolution des plaques d’athérosclérose chez les humains. Pour contourner cette limitation, les chercheurs ont utilisé des modèles de souris soumises à des régimes alimentaires contenant des proportions de protéines équivalentes à celles administrées aux volontaires de l’étude (15 et 22% des calories totales) et qui stimulent de façon similaire l’activité de mTOR dans les monocytes/macrophages.
Après seulement 8 semaines d’une alimentation riche en protéines, ils ont observé que le nombre de plaques au niveau de l’aorte était fortement augmenté et que celles-ci étaient infiltrées par un plus grand nombre de macrophages. Le volume de la zone nécrotique au centre des plaques, contenant des débris cellulaires, était également beaucoup plus important, fort possiblement en raison d’un nombre important de cellules spumeuses mortes. Selon les résultats antérieurs obtenus par le même groupe, il est fort probable que cette mort cellulaire soit une conséquence directe de l’inhibition de l’autophagie associée à l’activation de mTOR, plus précisément la mitophagie (l’autophagie des mitochondries).
L’ensemble de ces résultats suggèrent donc qu’un apport élevé en protéines entraine une suractivation de mTOR, la mort des macrophages infiltrés dans la paroi artérielle et une accélération du développement de l’athérosclérose. La quantité de protéines requises pour mettre ce processus en branle est cependant assez élevée, bien au-delà de l’apport nutritionnel recommandé de 0,8 g par kg par jour (Figure 7). Des apports quotidiens plus élevés, comme ceux recommandés pour les personnes actives et/ou âgées (1-1,2 g par kg) ne semblent pas avoir non plus d’effets majeurs sur le risque cardiovasculaire, ce qui est rassurant. Par contre, les données suggèrent que le 20-25 % de la population qui consomme des quantités très importantes de protéines (≥ 1,4 g par kg, soit environ ≥ 20 % des calories totales) présente un risque cardiovasculaire beaucoup plus élevé.
Plus de protéines végétales
Un point très important soulevé par les résultats de l’étude est que l’effet athérogénique des quantités élevées de protéines semble être essentiellement causé par un seul acide aminé, la leucine. Ceci est particulièrement intéressant, car la leucine est beaucoup plus abondante dans les sources de protéines animales que chez les végétaux (voir le Tableau 1), ce qui pourrait expliquer pourquoi ce sont seulement les protéines animales qui ont été associées à une hausse du risque de maladies cardiovasculaires et de diabète de type 2 dans les études épidémiologiques. En plus de respecter les apports nutritionnels recommandés (entre 0,8 et 1,2 g par kg par jour), une façon évidente de réduire l’impact négatif d’un apport élevé en protéines est donc de mieux répartir les sources de protéines, en augmentant la proportion qui provient d’aliments d’origine végétale. Cela en vaut vraiment la peine : une étude a par exemple montré que la substitution de seulement 3 % des calories provenant de protéines animales (les viandes rouges et charcuteries, en particulier) par l’équivalent en protéines d’origine végétale est associée à une réduction importante (34 %) du risque de mortalité prématurée.
| Sources animales | Sources végétales | ||||
|---|---|---|---|---|---|
| Aliment | Portion | Leucine (mg) | Aliment | Portion | Leucine (mg) |
| Bœuf (surlonge) | 85 g | 2180 | Tofu | 100 g | 1370 |
| Poulet (cuisse) | 85 g | 2031 | Pâte alimentaire | 100 g | 1033 |
| Thon (conserve) | 85 g | 1883 | Pain | 100 g | 691 |
| Poulet (poitrine) | 85 g | 1661 | Beurre d’arachide | 30 g | 440 |
| Jambon cuit | 85 g | 1440 | Pois verts | ½ tasse | 234 |
| Saumon | 85 g | 1272 | Maïs | ½ tasse | 207 |
| Fromage (cheddar) | 50 g | 1000 | Riz (grain long) | ½ tasse | 183 |
| Yogourt grec | ¾ tasse | 707 | Jus d’orange | 1 tasse | 139 |
| Oeuf | 1 | 541 | Brocoli | ¾ tasse | 133 |
| Lait (2%) | 1 tasse | 377 | Tomates | ½ tasse | 45 |
Tableau 1. Contenu en leucine de différents aliments couramment consommés. Les données proviennent de Rondanelli et coll. (2021) et du USDA Nutrient Database-Leucine (2018). Notez que l’apport nutritionnel recommandé pour la leucine est de 42 mg par kg par jour, soit environ 3000 mg pour un adulte moyen de 70 kg. La hausse du risque cardiovasculaire rapportée dans l’étude est observée à 1,5 g de protéine par kg (100 g pour un adulte de 70 kg), ce qui correspond à environ 9000 mg de leucine, trois fois l’apport recommandé.
Il y a encore malheureusement beaucoup de réticence dans l’adoption des végétaux comme source de protéines. On pense généralement, à tort, que l’apport en acides aminés peut être insuffisant dans les régimes végétariens; pourtant il est clairement démontré que les quantités et les proportions d’acides aminés consommées par les végétariens et les végétaliens sont généralement plus que suffisantes pour satisfaire et dépasser les besoins individuels quotidiens, à condition qu’une variété raisonnable d’aliments soit consommée et que les besoins énergétiques soient satisfaits. La croyance selon laquelle certains aliments végétaux « manquent » d’acides aminés spécifiques est fausse : tous les aliments végétaux contiennent les 20 acides aminés, y compris les 9 acides aminés essentiels. C’est le profil de distribution de certains de ces acides aminés qui est moins optimal dans les aliments végétaux que dans ceux d’origine animale. Par exemple, la lysine est présente dans les céréales dans des proportions bien inférieures aux proportions optimales pour les besoins humains, tandis que les quantités d’acides aminés soufrés (méthionine et cystéine) dans les légumineuses sont légèrement inférieures à l’apport optimal. Pour être carencée en certains acides aminés, il faudrait donc qu’une personne mange exclusivement du riz ou des haricots chaque jour, ce qui est évidemment improbable. En réalité, un régime alimentaire normal, même minimalement varié (ce qui est généralement le cas dans les pays riches), permet d’obtenir un apport adéquat de l’ensemble des acides aminés essentiels. Il est d’ailleurs utile de rappeler que les habitants de l’île d’Okinawa, où se trouve la plus forte proportion de centenaires au monde, mangent relativement peu de protéines (9 % des calories totales) et qu’une forte proportion de ces protéines proviennent des végétaux.
