Dr Josep Iglesies-Grau, M.D., Ph.D.
Centre de recherche et Centre ÉPIC, Institut de cardiologie de Montréal. Département de Médecine, Université de Montréal, Montréal, Québec, Canada, Département de Nutrition, Université de Montréal, Montréal, Québec, Canada
Voir tous les articlesEn bref
- Il est difficile de perdre du poids, et surtout de maintenir ces pertes à plus long terme, en raison d’une série d’adaptations du corps qui cherche à combattre farouchement la disparition de cette réserve d’énergie et à conserver le poids de départ.
- Ce phénomène est aussi observé pour les nouveaux agonistes du GLP-1 (Ozempic, Mounjaro), avec une reprise importante du poids perdu qui survient après l’arrêt des traitements.
- La prévention des nombreuses maladies qui découlent du surpoids ne peut donc pas reposer uniquement sur la prise de médicaments: une alimentation saine, principalement composée de végétaux et dépourvue d’aliments industriels hypercaloriques, demeure absolument incontournable pour la prise en charge à long terme de l’obésité.
Il est maintenant incontestable que l’excès d’adiposité est un important facteur de risque des maladies chroniques qui touchent une proportion importante de la population, incluant les maladies cardiovasculaires, le diabète de type 2, les démences ainsi que plusieurs types de cancers. Pour les personnes qui souffrent d’obésité, la perdre du poids représente donc une avenue très intéressante pour diminuer l’incidence et la progression de plusieurs de ces pathologies. Ceci est particulièrement vrai en ce qui concerne les maladies cardiovasculaires, où une perte de poids aussi faible que 5 % du poids initial peut renverser de nombreux effets cardiométaboliques néfastes liés à un excès d’adiposité.
Les études récentes montrent clairement que la seule véritable façon de parvenir à une perte significative de poids, et surtout de maintenir ces pertes à long terme, repose en majeure partie sur une réduction durable de l’apport énergétique. Cependant, cet objectif est difficile à atteindre pour la plupart des gens, particulièrement dans des environnements où l’offre alimentaire est abondante et facilement accessible. En conséquence, même si ces régimes permettent généralement d’obtenir une perte de poids à court terme, cette perte est très souvent temporaire et une reprise pondérale partielle ou complète peut survenir avec le temps, quelles que soient les approches nutritionnelles utilisées.
La mémoire de l’obésité
Contrairement à certaines perceptions encore répandues, ce regain de poids n’a absolument rien à voir avec un supposé manque de bonne volonté des personnes vivant avec un excès de poids. La recherche des dernières décennies a clairement montré que la perte de graisse déclenche une série d’adaptations métaboliques, hormonales et neurologiques très complexes destinées à combattre farouchement la disparition de cette réserve d’énergie et à conserver le poids de départ. Autrement dit, le corps possède une forme de « mémoire de l’obésité » qui rend extrêmement difficile le maintien des pertes de poids à long terme, quelle que soit la façon utilisée pour réduire le poids corporel. Au moins quatre grands facteurs participent à cette mémoire (Figure 1) :
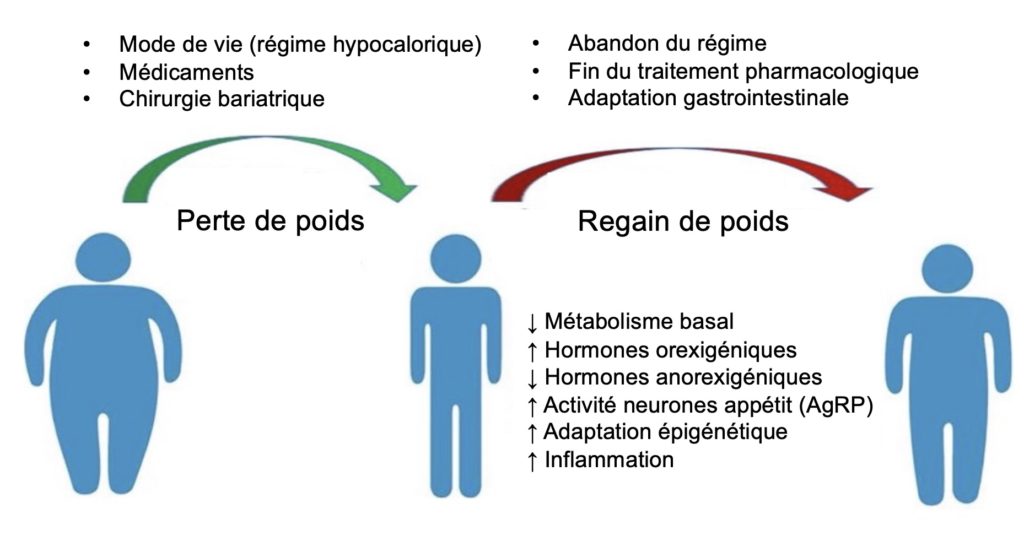
- Réduction du métabolisme de base. De 60 à 75 % de notre dépense énergétique totale provient du métabolisme basal, c’est-à-dire la quantité d’énergie qui est dépensée pour assurer les fonctions vitales au repos. Après une perte de poids, cette dépense énergétique de base peut diminuer énormément (jusqu’à 700 kcal par jour), de sorte que même un apport calorique normal peut excéder les besoins du corps et favoriser le surpoids. Ce phénomène est une adaptation qui s’est forgée au fil de l’évolution pour survivre à la famine : en réponse à une baisse drastique des calories disponibles (comme dans le cas d’un régime hypocalorique sévère), le métabolisme basal devient beaucoup plus efficace et produit davantage d’énergie (sous la forme ATP) avec moins de pertes de chaleur, ce qui permet de préserver les réserves énergétiques à long terme.
- Augmentation de l’appétit. La réponse à une perte de poids importante, synonyme de famine pour le cerveau, est également caractérisée par des modifications profondes et persistantes des hormones impliquées dans la régulation de l’appétit. Par exemple, on observe une augmentation des hormones stimulatrice (orexigéniques) comme la ghréline et une réduction parallèle des hormones qui normalement suppriment l’appétit (anorexigéniques) comme PYY, la cholécystokinine (CCK), l’amyline et la leptine. Ces variations compensatoires entraînent une augmentation de l’appétit difficile à contrôler, caractérisée par des fringales, une hypersensibilité à l’odeur ou à la simple vision d’une source de nourriture et un plaisir démesuré provoqué par sa consommation (valeur hédonique). La perte de poids semble également provoquer une forte stimulation des neurones orexigènes (AgRP) au niveau de l’hypothalamus, déclenchant ainsi une augmentation durable de l’apport alimentaire et une reprise du poids perdu.
- Mémoire génétique de l’obésité. L’exposition répétée à un excès de calories cause une hypertrophie des cellules adipeuses (les adipocytes) pour parvenir à emmagasiner ce surplus d’énergie. Les adipocytes sont des cellules extrêmement flexibles et peuvent modifier l’expression de plusieurs gènes pour permettre cette croissance. Ces changements sont conservés en mémoire (adaptation épigénétique), de sorte qu’après la fin d’un traitement pour la perte de poids, les adipocytes sont déjà « programmés » pour emmagasiner un surplus d’énergie si le nombre de calories excède les besoins de l’organisme.
- Inflammation au niveau des adipocytes. L’expansion du tissu adipeux peut être interprétée comme une agression par le système immunitaire, ce qui entraîne l’infiltration de plusieurs cellules pro-inflammatoires et la création d’un climat d’inflammation chronique qui affecte la fonction des adipocytes et favorise la croissance anormale du tissu adipeux au-delà des limites normalement imposées par l’enveloppe du tissu (la matrice extracellulaire). Ces cellules inflammatoires demeurent présentes dans le tissu adipeux même après une perte de poids importante, de sorte que l’exposition subséquente à un excès de calories (causée par les facteurs métaboliques et hormonaux mentionnés plus haut) va causer une accumulation de graisse encore plus rapide que chez des adipocytes qui n’ont jamais été exposés à l’obésité et ainsi mener à un regain de poids post-amaigrissement (Figure 2). Des études récentes suggèrent que ce dérèglement de l’inflammation en réponse à l’obésité pourrait durer plusieurs années en raison d’une adaptation durable des cellules de l’immunité adaptative (lymphocytes T CD4+) à l’accumulation excessive de graisse dans le tissu adipeux.
Pour toutes ces raisons, la réduction durable du poids corporel est généralement un objectif très difficile à atteindre pour plusieurs personnes, surtout lorsque le niveau d’adiposité est important .
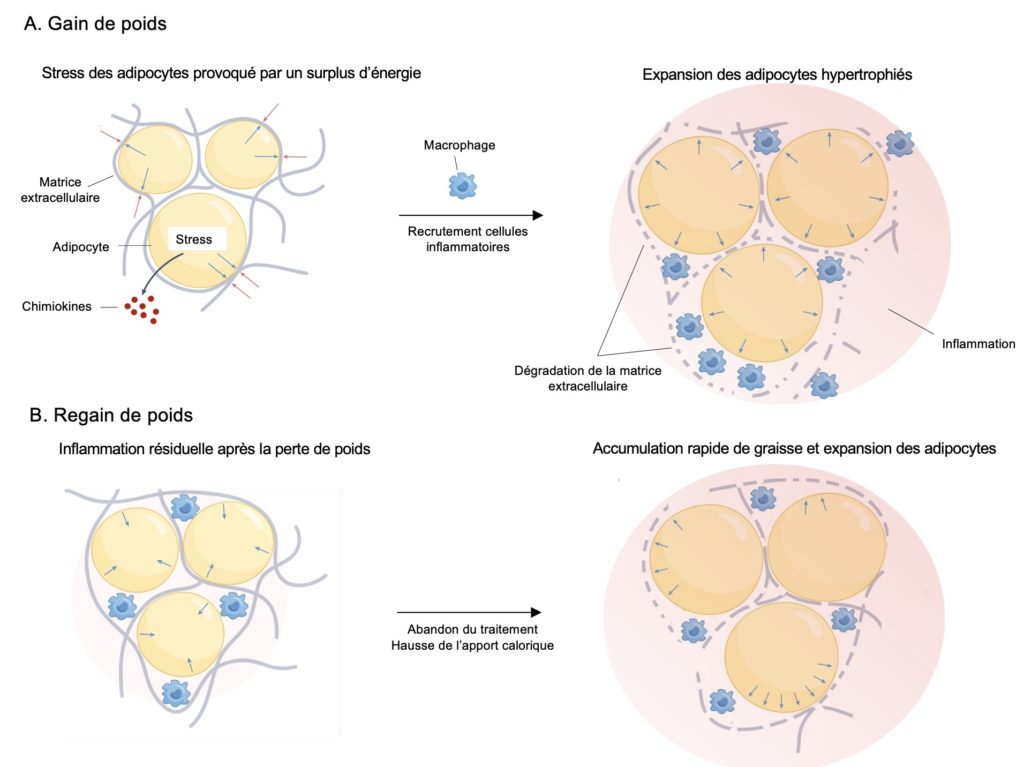
A. Un bilan énergétique positif entraîne l’expansion des adipocytes, ce qui génère un stress aux points de contact avec la matrice extracellulaire qui entoure le tissu adipeux et empêche son expansion (flèches bleues et rouges). Des chimiokines sont alors sécrétées par les adipocytes pour attirer les cellules inflammatoires (macrophages), et ce recrutement provoque une inflammation locale (illustrée en rouge) et la sécrétion d’enzymes qui dégradent la matrice, affaiblissant celle-ci et permettant une expansion accrue des adipocytes.
B. Après une perte de poids, la taille des adipocytes diminue et la matrice régénérée se resserre autour des adipocytes atrophiés. Cependant, certains macrophages demeurent dans le tissu adipeux et, en cas de nouvelle suralimentation, sont déjà sur place pour sécréter les enzymes de dégradation de la matrice, ce qui favorise la prolifération rapide des adipocytes et la reprise de poids. Adapté de van Baak et Mariman (2023).
Effet yo-yo
En plus d’être extrêmement décourageants, ces regains de poids semblent aussi avoir des effets négatifs sur la santé, surtout lorsqu’ils se produisent à répétition. Ces fluctuations pondérales répétées, qu’on appelle « effet yo-yo » (par analogie au jouet qui monte et descend), peuvent toucher jusqu’à 50 % de la population adulte et plusieurs études (mais pas toutes, voir ici par exemple) ont rapporté un risque accru de différentes pathologies chez les personnes dont le poids fluctue le plus. Par exemple, des méta-analyses récentes ont montré que les fluctuations de poids augmentent le risque d’hypertension artérielle (HTA), de maladies cardiovasculaires, de diabète de type 2 (DT2), et de mortalité toutes causes confondues. Les mécanismes en cause demeurent à être identifiés, mais il a été proposé dans le cas des maladies cardiovasculaires que les cycles répétés de perte-regain de poids entraînaient des fluctuations anormales de plusieurs facteurs de risque comme la pression artérielle, la fréquence cardiaque, le travail cardiaque, l’activité sympathique, la glycémie et le profil lipidique. Le stress induit par les variations répétées de ces variables imposerait une charge supplémentaire au cœur et pourrait donc entraîner des lésions vasculaires menant au développement de l’athérosclérose.
Les agonistes du GLP-1
La popularité récente des agonistes du GLP-1 comme le semaglutide (Ozempic, Wegovy) et le tirzepatide (Mounjaro, Zepbound) permet de bien mettre en lumière ce problème du regain de poids après une perte de poids induite par le traitement. Comme nous l’avons décrit plus en détail, ces médicaments sont des analogues d’une hormone sécrétée par l’intestin (GLP-1) qui ont été initialement développés pour améliorer le contrôle de la glycémie chez les patients atteints du diabète de type 2. La différence fondamentale entre ces deux classes d’agonistes est que le semaglutide est un agoniste simple du GLP-1, tandis que le tirzepatide est un agoniste double, c’est-à-dire qu’il présente une structure hybride qui lui permet d’activer à la fois les récepteurs du GLP-1 et celui d’une autre hormone, le GIP.
Ces médicaments sont maintenant surtout connus pour leurs effets marqués sur la perte de poids, avec des réductions du poids corporel pouvant atteindre 15-20 % dans certains cas, soit beaucoup plus que les pertes enregistrées par des modifications du mode de vie (régimes, exercice) ou par les premières générations de médicaments utilisés pour la gestion du poids (Figure 3). L’efficacité des médicaments GLP-1 pour la perte de poids semble surtout due à leur action directe sur les processus impliqués dans le contrôle du comportement alimentaire, notamment une diminution notable de l’appétit, réduisant l’apport calorique de l’ordre de 30 % et ralentissant également la vidange gastrique, ce qui favorise une sensation de satiété plus précoce et plus prolongée, parfois accompagnée de nausées, même après de petits repas. C’est donc l’important déficit énergétique qui découle du mode d’action de ces médicaments qui serait directement responsable des pertes de poids importantes observées dans les études, confirmant que c’est une diminution significative de l’apport calorique qui détermine en grande partie la perte de poids.
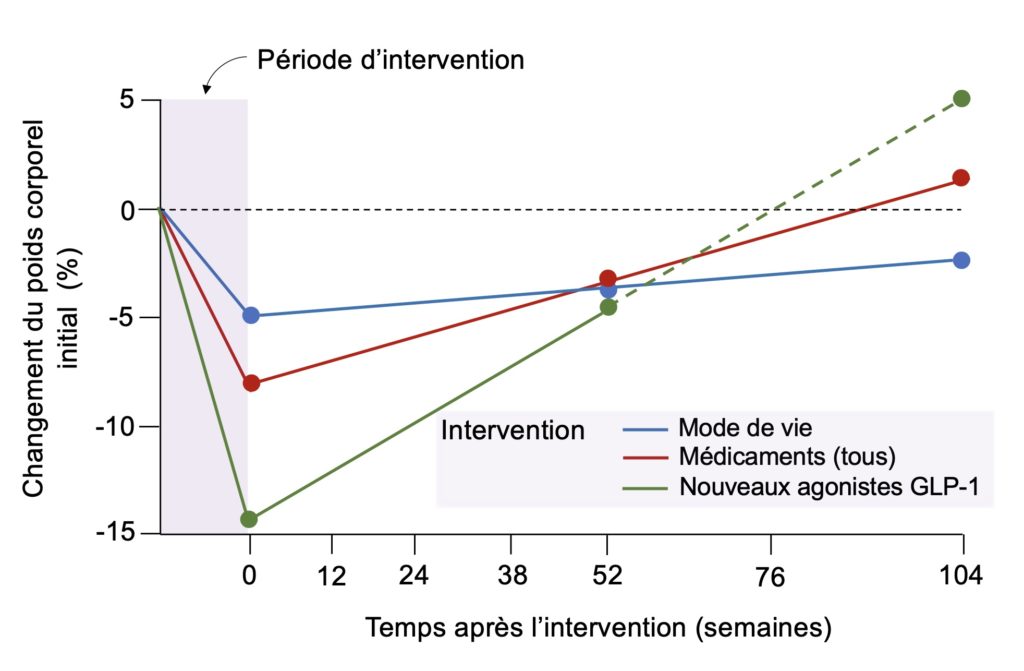
Malgré leur efficacité à court terme, les agonistes du GLP-1 présentent cependant le même problème qui affecte l’ensemble des traitements pour la perte de poids à long terme, c’est-à-dire que l’arrêt du traitement est généralement suivi d’un regain de poids considérable, avec environ les deux tiers du poids perdu repris dans l’année qui suit (Figure 3). En conséquence, l’amélioration de plusieurs paramètres de santé procurée par la perte de poids peut alors être renversée par une détérioration significative de plusieurs paramètres associés au surpoids, notamment la pression artérielle et le contrôle adéquat de la glycémie.
Cette situation soulève certains enjeux cliniques, dans la mesure où il est difficilement concevable d’administrer ces médicaments sur de très longues périodes pour éviter ces rechutes. D’une part, la compliance à ces médicaments reste en ce moment assez modérée, avec moins de 50 % des personnes qui poursuivent le traitement au-delà d’un an, principalement en raison d’effets secondaires assez prononcés (notamment gastro-intestinaux, comme les nausées). D’autre part, la perte majeure d’appétit chez les personnes traitées augmente considérablement le risque de malnutrition, avec une proportion importante de patients qui n’atteignent pas les seuils minimaux recommandés pour plusieurs nutriments essentiels. On a aussi noté chez les personnes présentant des antécédents de troubles de santé mentale ou de troubles alimentaires une hausse du risque de certains désordres alimentaires (l’anorexie, par exemple), et une vigilance clinique particulière est donc requise pour éviter une possible exacerbation de ces comportements alimentaires problématiques.
En somme, malgré l’enthousiasme actuel généré par les agonistes du GLP-1, ces médicaments ne peuvent être présentés comme une solution miracle contre un problème aussi complexe que l’obésité. Bien qu’une perte de poids importante, même temporaire, puisse apporter certains bienfaits pour la santé, celles qui utilisent ces agonistes devraient être informées des limites de ces médicaments, notamment du taux élevé d’abandon du traitement et du risque de reprise pondérale après leur arrêt.
Combiner traitements, alimentation et environnement favorable
La hausse fulgurante du nombre de personnes en surpoids observée au cours des dernières décennies montre clairement que l’épidémie actuelle d’obésité est étroitement liée aux transformations de nos modes de vie, avec un rôle important joué par l’omniprésence des aliments ultratransformés dans l’alimentation, la perte progressive des habitudes alimentaires et culinaires traditionnelles, ainsi qu’à l’augmentation de la sédentarité et de l’inactivité physique. Un retour aux sources, basé sur une alimentation saine principalement composée de végétaux et dépourvue d’aliments industriels hypercaloriques, demeure donc absolument incontournable pour la prise en charge de l’obésité. Sans remplacer ces prérequis, les médicaments GLP-1 peuvent néanmoins jouer un rôle complémentaire en permettant à certaines personnes d’obtenir une perte de poids significative, parfois difficilement atteignable auparavant. L’adoption parallèle d’une alimentation plus saine pendant le traitement, combinée aux nombreux bénéfices physiques et psychologiques procurés par la perte de poids, pourrait alors servir de tremplin pour conserver ce nouveau mode de vie et éviter les regains de poids associés à l’arrêt du traitement.
Enfin, la société a aussi un rôle important à jouer pour modifier l’environnement obésogène dans lequel nous vivons. Des mesures de santé publique efficaces, comme la taxation des boissons sucrées, un étiquetage alimentaire clair et des politiques facilitant l’accès aux fruits, aux légumes et aux aliments frais, devraient être mises en place afin de soutenir durablement l’amélioration de la qualité de l’alimentation et de rendre les choix favorables à la santé plus simples, plus accessibles et plus durables. Car prévenir l’obésité ne peut pas reposer uniquement sur les individus ni dépendre uniquement de la prise de médicaments: cela exige aussi de bâtir un environnement qui rend la santé possible.
